La batterie sodium-ion (NIB ou SIB) est un type de batterie rechargeable qui utilise des ions sodium (Na+) comme porteurs de charge. Son principe de fonctionnement et la construction des cellules sont presque identiques à ceux des types de batteries lithium-ion (LIB), mais remplacent le lithium par du sodium.
Les batteries sodium-ion représentent une alternative potentielle aux technologies à base de batteries lithium, principalement en raison du coût plus faible du sodium et de sa meilleure disponibilité. Puisque les SIB utilisent des matériaux abondants et bon marché, on s’attend à ce qu’ils soient moins coûteux que les LIB. Les impacts environnementaux des SIB sont également plus faibles. Bien que les SIB soient plus lourds et plus volumineux que les LIB, ils sont réalisables pour les systèmes de stockage d’énergie stationnaires où le poids et le volume sont moins cruciaux.
Les SIB ont suscité un intérêt académique et commercial dans les années 2010 et 2020, principalement en raison de la répartition géographique inégale, de l’impact environnemental élevé et du coût élevé de nombreux matériaux nécessaires aux batteries lithium-ion. Les principaux parmi eux sont le lithium, le cobalt, le cuivre et le nickel, qui ne sont pas strictement requis pour de nombreux types de batteries sodium-ion. Le plus grand avantage des batteries sodium-ion est l’abondance naturelle de sodium. Les défis à l’adoption des SIB incluent une faible densité d’énergie et des cycles charge-décharge insuffisants.
En 2022, les batteries sodium-ion n’étaient pas encore devenues commercialement significatives, mais cela pourrait changer lorsque le plus grand fabricant mondial de batteries a annoncé le début de la production de masse des SIB en 2023. Cette technologie n’est pas mentionnée dans un rapport de la United States Energy Information Administration sur les technologies de stockage par batterie. De plus, aucun véhicule électrique n’utilise de batteries sodium-ion… pas encore.
L’histoire
Le développement des batteries sodium-ion a eu lieu dans les années 1970 et au début des années 1980. Cependant, dans les années 1990, les batteries lithium-ion avaient un potentiel commercial plus démontré, ce qui a fait baisser l’intérêt pour les batteries sodium-ion. Au début des années 2010, les batteries sodium-ion ont connu une résurgence, principalement grâce à l’augmentation du coût des matières premières pour batteries lithium-ion.
Principe de fonctionnement
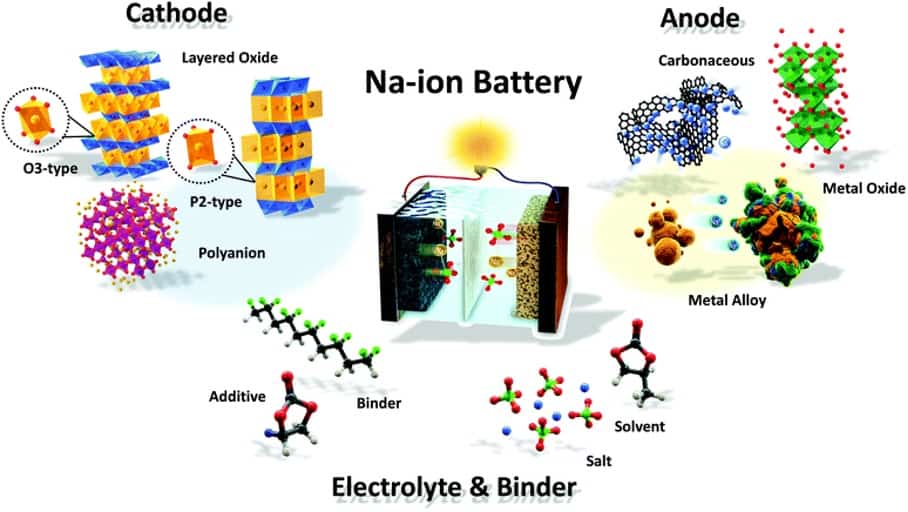
Les cellules SIB sont constituées d’une cathode à base d’un matériau contenant du sodium, d’une anode (pas nécessairement à base de sodium) et d’un électrolyte liquide contenant des sels de sodium dissociés dans des solvants polaires protiques ou aprotiques. Lors de la charge, les ions sodium se déplacent de la cathode vers l’anode tandis que les électrons circulent dans le circuit externe. Lors de la décharge, le processus inverse se produit.
Matériaux (anodes, cathodes et électrolytes)
En raison des propriétés physiques et électrochimiques du sodium, les SIB nécessitent d’autres matériaux que ceux utilisés pour les LIB.
Anodes
Les SIB utilisent du carbone dur, un matériau carboné désordonné constitué d’un carbone non graphitisable, non cristallin et amorphe. La capacité du carbone dur à absorber le sodium a été découverte en 2000. Cette anode a montré une puissance de 300 mAh/g avec un profil potentiel incliné au-dessus de \u20120,15 V par rapport à Na/Na+. Il représente environ la moitié de la capacité et un profil potentiel plat (un plateau potentiel) en dessous de la valeur de Na/Na+. Les anodes en graphite pour les LIB offrent des capacités typiques de 300 à 360 mAh/g. La première cellule sodium-ion utilisant du carbone dur a été démontrée en 2003 et a montré une tension moyenne de 3,7 V lors de la décharge. Le carbone dur est préféré en raison de son excellente combinaison de capacité, de potentiels de travail (plus faibles) et de stabilité en cycle.
Cathodes
Les cathodes sodium-ion stockent le sodium par intercalation. En raison de leur densité de prise élevée, de leurs potentiels de fonctionnement élevés et de leurs grandes capacités, les cathodes à base d’oxydes de métaux de transition de sodium ont attiré la plus grande attention. Pour maintenir les coûts bas, la recherche tente de minimiser les éléments coûteux tels que le Co, le Cr, le Ni ou le V. Un oxyde de typeP2 Na 2/3Fe1/2Mn1/2O2 provenant de ressources terrestres abondantes en Fe et Mn peut stocker de manière réversible 190 mAh/g à une tension de décharge moyenne de 2,75 V, contre Na/Na+ utilisant le couple redox Fe3+/4+ – équivalent ou meilleur que les cathodes lithium-ion commerciales telles que LiFePO4 ouLiMn 2O 4. Cependant, sa nature carente en sodium a réduit la densité énergétique. Des efforts importants ont été déployés pour développer des oxydes plus riches en Na. Les matériaux cathodiques Na0,67Ni0,3−xCuxMn 0,7O2 substitués par le cuivre ont montré une grande capacité réversible avec une meilleure rétention de capacité. Contrairement à l’électrode sans cuivre Na0,67Ni0,3−xCuxMn0,7O2, les cathodes substituées par le Cu telles que préparées offrent un meilleur stockage du sodium.
La recherche a également examiné les cathodes basées sur les polyanions. Ces cathodes offrent une densité de tap plus faible, réduisant la densité d’énergie en raison de l’anion encombrant. Cela peut être compensé par la liaison covalente plus forte du polyanion, qui a un impact positif sur la durée de vie et la sécurité du cycle. Parmi les cathodes à base de polyanions, le phosphate de sodium vanadium et le fluorophosphate ont démontré une excellente stabilité au cycle et, dans ce dernier, une capacité acceptable élevée (« mAh/g) » à des tensions moyennes de décharge élevées (\u20123,6 V vs Na/Na+).
Électrolytes
Les batteries sodium-ion peuvent utiliser des électrolytes liquides et non liquides. La fenêtre de stabilité électrochimique limitée de l’eau entraîne des tensions plus faibles et des densités énergétiques limitées. Les solvants aprotiques polaires esters carbonatés non liquides prolongent la plage de tension. Celles-ci incluent le carbonate d’éthylène, le carbonate de diméthyle, le carbonate de diéthyle et le carbonate de propylène. L’électrolyte non liquide le plus utilisé utilise l’hexafluorophosphate de sodium comme sel dissous dans un mélange de ces solvants. De plus, les additifs électrolytiques peuvent améliorer les indicateurs de performance.
Comparaison
Les batteries sodium-ion présentent plusieurs avantages par rapport aux technologies concurrentes. Comparées aux batteries lithium-ion, les batteries sodium-ion ont un coût légèrement inférieur, une densité énergétique légèrement inférieure, de meilleures caractéristiques de sécurité et des caractéristiques de livraison de puissance similaires.
Le tableau ci-dessous compare la performance générale des NIB par rapport aux deux technologies de batteries rechargeables établies actuellement sur le marché : la batterie lithium-ion et la batterie rechargeable au plomb.
Batterie sodium-ion | Batterie lithium-ion | Batterie au plomb | |
Coût par kilowattheure de capacité | 40–77 $ | 137 $ (moyenne en 2020). | 100–300 $ |
Densité d’énergie volumétrique | 250–375 W·h/L, basés sur des prototypes | 200–683 W·h/L | 80–90 W·h/L |
75–165 W·h/kg, basé sur des prototypes et des annonces de produits | 120–260 P·h/kg | 35–40 Wh/kg | |
Cycles à 80 % de profondeur de débit | Des centaines à des milliers. | 3,500 | 900 |
Sécurité | Faible risque pour les batteries aqueuses, risque élevé de Na dans les batteries au carbone | Haut risque | Risque modéré |
Matériaux | Abondante en Terre | Rare | Toxique |
Stabilité en cycle | Élevée (auto-écoulement négligeable) | Élevée (auto-écoulement négligeable) | Modéré (haute auto-écoulement) |
Efficacité aller-retour en courant continu | jusqu’à 92 % | 85–95% | 70–90% |
Plage de température | −20 °C à 60 °C | Acceptable : −20 °C à 60 °C. Optimal : 15 °C à 35 °C | −20 °C à 60 °C |
Jongia Mixing Technology est toujours en mesure d’aider à guider la sélection de la configuration de l’agitateur.
Il suffit de contacter Jongia et de demander de l’aide.
Nous sommes toujours disponibles pour vos demandes de mixeurs.
Contactez-nous à : info@jongia.com ou consultez d’autres articles sur les batteries ion-lithium sur notre page piles.
Cet article a été rédigé en utilisant certaines informations provenant des sites suivants :
Page Wikipédia sur la batterie sodium-ion
https://pubs.rsc.org/en/content/articlelanding/2017/cs/c6cs00776g
Contactez notre équipe spécialisée pour toutes vos questions

Teun van der Spek
Responsable des ventes régionales
Des questions techniques ?

Jan Siert Tjeerdsma
Chef de projet
Spécialiste technique
Articles connexes

Quel est le processus de recyclage du lithium
Les batteries lithium-ion commerciales actuelles contiennent principalement des oxydes ou phosphates de métaux de transition, de l’aluminium, du cuivre, du graphite, des électrolytes organiques contenant des sels de lithium nocifs, et d’autres produits chimiques. Par conséquent, le recyclage et la
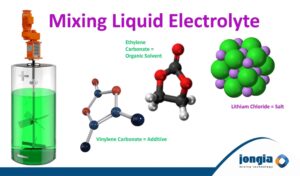
Mélange d’électrolytes pour batteries ion-lithium
L’électrolyte, à la base des batteries ion-lithium, joue un rôle clé dans le transport des ion-lithium positifs entre la cathode et l’anode, et par conséquent dans la performance de charge et de décharge de la batterie. Il faut donc vérifier

Mélanger la bonne boue ion-lithium est un vrai défi !
Les technologies de batteries à base de lithium pour véhicules électriques utilisent des ions-lithium comme porteurs de charge. Selon les exigences techniques de l’application, le lithium est utilisé avec diverses chimies telles que le graphite pour l’anode ainsi que des




